Gefäßchirurgie 7: 171-179
(Prof. Dr. Viola Hach-Wunderle, Prof. Dr. W Hach)
Die sekundäre Leitveneninsuffizienz
W. Hach, V. Hach-Wunderle und F. Präve
Die sekundäre Leitveneninsuffizienz gilt als die wichtigste Komplikation der Stammvarikose. Sie ist die Ursache für den komplizierten Krankheitsverlauf im Sinne des chronischen venösen Stauungssyndroms. Ursprünglich wurde sie als eine Röntgendiagnose definiert, heute ist sie auch durch die moderne Duplexsonographie festzustellen. Zusätzlich Informationen liefern die physikalische Meßverfahren. Für die Therapie kommt nur die komplexe extrafasziale Sanierungsoperation in Betracht. Die physikalische Nachbehandlung hat eine große Bedeutung.
 Friedrich Trendelenburg (1844-1924). Ordinarius für Chirurgie in Rostock, Bonn und Leipzig. Entdecker des Privatkreislaufs bei der primären Varikose (1891).
Friedrich Trendelenburg (1844-1924). Ordinarius für Chirurgie in Rostock, Bonn und Leipzig. Entdecker des Privatkreislaufs bei der primären Varikose (1891).
Heute hat die sekundäre Leitveneninsuffizienz als Komplikation eines pathologischen Rezirkulationskreises im Rahmen der Stamm- und Perforansvarikose eine allgemeine Akzeptanz gefunden. Nach ihrer Entdeckung 1980 (10) forderte sie lebhafte Proteste durch namhafte Phlebologen heraus. In der hundertjährigen Geschichte einer wissenschaftlichen Betrachtung der Krampfaderkrankheit war es einfach nicht vorstellbar, dass die oberflächlich liegenden Varizen manchmal so schwere Veränderungen im tiefen Venensystem hervorrufen können, dass sie sogar zum arthrogenen Stauungssyndrom oder im extremen Fall zum chronischen venösen Kompressionssyndrom führen. Heute findet das Thema ein anhaltendes wissenschaftliches Interesse (2, 13, 16, 18)
Begriffsbestimmung
Im Jahre 1891 beschrieb Friedrich Trendelenburg den Privatkreislauf bei der Stammvarikose der V. saphena magna (23). Sobald die Muskeln in Thätigkeit sind, ...wird der Blutstrom in den tiefen Venen beträchtlich schneller gehen; in den Verbindungsvenen xx wird das Blut abgesaugt werden. Es wird nicht ausbleiben können, dass das Blut aus dem Reservoir der gefüllten Saphena nachfliesst und oben aus der Femoralis wieder ersetzt wird, so dass es sich in diesem Falle sozusagen um einen privaten Kreislauf handelt
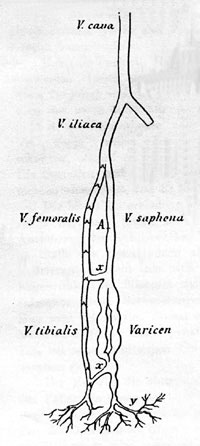 Darstellung des Privatkreislaufes einer Stammvarikose der V. saphena magna durch Trendelenburg 1892 (23).
Darstellung des Privatkreislaufes einer Stammvarikose der V. saphena magna durch Trendelenburg 1892 (23).
Fischer und Siebrecht haben 1970 festgestellt, dass die schwere Varikose zur Erweiterung der tiefen Leitvenen führt. Die Autoren sahen diesen Effekt aber nur an den Unterschenkelgefäßen (3). Schneider und Fischer nahmen 1969 eine funktionelle Insuffizienz der Wadenmuskelpumpe als Ursache an, die durch eine Überlagerung ihrer Förderkapazität infolge des Pendelblutvolumens zustande kommt. Eine kausale Rolle sollten dabei außerdem die Erschwerung der Blutbeschleunigung durch die erhöhte Blutmenge und die Vermehrung des Totraums spielen (19). Diese Konzepte haben auch in der modernen Vorstellung zur Pathogenese der sekundären Leitveneninsuffizienz eine wichtige Bedeutung.
Hach et al (10) haben bei ihren phlebographischen Untersuchungen die morphologischen Veränderungen hauptsächlich in der poplitealen und femoralen Strombahn gefunden und deshalb eine sekundäre Popliteal- und Femoralveneninsuffizienz definiert. Mellmann kam 1981 aufgrund röntgenmorphometrischer Untersuchungen zu entsprechenden Ergebnissen, stellte darüber hinaus aber auch an den Leitvenen des Unterschenkels und in der Beckenregion pathologische Reaktionen fest (15). Der umfassende Terminus sekundäre Leitveneninsuffizienz (SLVI) wird der hämodynamischen Situation am besten gerecht. Inzwischen sind zahlreiche Veröffentlichungen zu dieser Thematik erschienen (2, 6, 11, 13, 16, 18). Die SLVI erklärt sich aus der modernen Theorie der Rezirkulationskreise und wird demnach auch bei einer Stammvarikose der V. saphena parva oder einer ausgeprägten isolierten Perforansvarikose gesehen (4)
 Dekompensierter Rezirkulationskreis als Ursache der CVI (9). Abschnitt 1: Stammvarikose mit rezirkulierendem Blutvolumen. Abschnitt 2: Übergang am distalen Insuffizienzpunkt in die obligate Seitenastvarikose. Abschnitt 3:Übertritt des rezirkulierten Blutvolumens über Vv. perforantes in das tiefe Venensystem. Abschnitt 4: Dilatation und Elongation der popliteofemoralen Strombahn mit Verlust der Klappenfunktion. Antegrade Strömungsinsuffizienz.
Dekompensierter Rezirkulationskreis als Ursache der CVI (9). Abschnitt 1: Stammvarikose mit rezirkulierendem Blutvolumen. Abschnitt 2: Übergang am distalen Insuffizienzpunkt in die obligate Seitenastvarikose. Abschnitt 3:Übertritt des rezirkulierten Blutvolumens über Vv. perforantes in das tiefe Venensystem. Abschnitt 4: Dilatation und Elongation der popliteofemoralen Strombahn mit Verlust der Klappenfunktion. Antegrade Strömungsinsuffizienz.
Im Rezirkulationskreis einer Stammvarikose der V. saphena magna oder parva fließt das Blut über den proximalen Insuffizienzpunkt nach distal zurück, tritt am unteren lnsuffizienzpunkt in die konjugierende Seitenastvarikose und dann über die Vv. perforantes wieder in das tiefe Venensystem ein. Solange keine SLVI vorliegt, wird von einem kompensierten Rezirkulationskreis gesprochen, im anderen Fall von der Dekompensation (8).
Heute definieren wir die sekundäre Leitveneninsuffizienz als Folge eines persistierenden Rezirkulationskreises bei der Stammvarikose oder Perforansvarikose, die für die Entstehung der chronischen venösen Insuffizienz mit allen Folgen und Komplikationen letztendlich verantwortlich zu machen ist.
Pathomorphologie und –physiologie
Am besten lassen sich die morphologischen und hämodynamischen Bedingungen der SLVI bei der aszendierenden Pressphlebographie und bei der seitenvergleichenden Betrachtung der entsprechenden Röntgenbilder erkennen und verstehen. Als phlebographische Kardinalsymptome (Tab. 1) sind die Erweiterung und die vermehrte Schlängelung der tiefen Leitvenen mit dem Verlust der Klappenfunktion zu nennen (4, 10).
| Tabelle 1: Röntgensymptome der sekundären Leitveneninsuffizienz |
| Dilatation der popliteo-femoralen Strombahn und fakultativ der Beckenstrombahn |
| Verlust der popliteo-femoralen Venenklappenfunktion |
| Verstärkte Abwinkelung am popliteo-femoralen Übergang |
| Schlängelung der V. femoralis superficialis |
| Antegrade Strömungsinsuffizienz mit Verwaschungseffekt |
Beweise für die kausalen Beziehungen der SLVI zur Stammvarikose ergaben sich einerseits aus der Langzeitbeobachtung des spontanen Krankheitsverlaufs mit phlebographischer Dokumentation. Ohne Behandlung nahm der Durchmesser der V. poplitea und der V. femoralis bei Patienten mit Stammvarikose der V. saphena magna im Stadium III und IV innerhalb 7,1 +/_ 2,8 Jahre durchschnittlich um 3 mm zu (22).
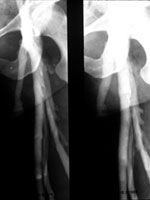 Entwicklung der sekundären Leitveneninsuffizienz bei einer 28-jährigen Frau mit Stammvarikose der V. saphena magna im Stadium III. Kasuistik der ersten Entdeckung der Krankheit am 18.9.1984. Links: Phlebographie vom 19.9.1978. V. femoralis superficialis suffizient, deutlich abgrenzbare Venenklappen. Rechts: Aufnahme nach 6 Jahren. Sekundäre Popliteal- und Femoralveneninsuffizienz. Erweiterung der V. femoralis superficialis und Verlust der Klappenfunktion. Ausbildung eines Ulcus cruris.
Entwicklung der sekundären Leitveneninsuffizienz bei einer 28-jährigen Frau mit Stammvarikose der V. saphena magna im Stadium III. Kasuistik der ersten Entdeckung der Krankheit am 18.9.1984. Links: Phlebographie vom 19.9.1978. V. femoralis superficialis suffizient, deutlich abgrenzbare Venenklappen. Rechts: Aufnahme nach 6 Jahren. Sekundäre Popliteal- und Femoralveneninsuffizienz. Erweiterung der V. femoralis superficialis und Verlust der Klappenfunktion. Ausbildung eines Ulcus cruris.
Andererseits bildete sich die SLVI nach einer operativen Behandlung der Stammvarikose weitgehend oder vollständig zurück.
Thomas wies schon 1893 für das Arteriensystem nach, daß eine Steigerung der Blutstromgeschwindigkeit zur Erweiterung des Gefäßlumens führt (Thomas´sche Gesetze) (20). Die Schlängelung von Gefäßen, betrachtet am Beispiel der arteriellen Kollateralen, entsteht durch eine Zunahme des Längenwachstums und manifestiert sich später als Dilatation. Ähnliche Auswirkungen hat auch eine Zunahme der Blutviskosität. Sind erst einmal Krümmungen im Gefäßverlauf entstanden, dann begünstigen strömungsdynamische Faktoren deren Progredienz. Entsprechende Untersuchungen über das Verhalten der tiefen Leitvenen bei Stammvarikose liegen nicht vor. Bjordal stellte durch direkte elektromagnetische Messungen an der insuffizienten V. saphena magna fest, daß beim Gehen ein zusätzliches, von den intrafaszialen Gefäßen zu bewältigendes Blutvolumen von 175 bis 500 ml/min entsteht (1).
Am Übergang der V. poplitea zur V. femoralis superficialis, also in Höhe des Adduktorenkanals, besteht normalerweise eine diskrete Abwinkelung der Gefäßachse von 155 bis 162°, die vom Lebensalter abhängig ist (4). Dieser Winkel wirkt bei einer Zunahme des rezirkulierenden Blutvolumens im Rahmen einer Stammvarikose der V. saphena magna gewissermaßen als Locus minoris resistentiae und reagiert im Stadium III mit einer Zuspitzung um durchschnittlich 10°, bzw. im Stadium IV um 16°.
 Beginnende sekundäre Leitveneninsuffizienz rechts (linkes Bild) bei Stammvarikose der V. saphena magna mit dekompensiertem Rezirkulationskreis III. Vergleich mit der gesunden Seite (rechtes Bild). Deutliche Erweiterung der popliteo-femoralen Strombahn rechts und Zunahme des popliteofemoralen Winkels. Klappenfunktion gerade noch erhalten. Darstellung durch aszendierende Pressphlebographie.
Beginnende sekundäre Leitveneninsuffizienz rechts (linkes Bild) bei Stammvarikose der V. saphena magna mit dekompensiertem Rezirkulationskreis III. Vergleich mit der gesunden Seite (rechtes Bild). Deutliche Erweiterung der popliteo-femoralen Strombahn rechts und Zunahme des popliteofemoralen Winkels. Klappenfunktion gerade noch erhalten. Darstellung durch aszendierende Pressphlebographie.In seltenen Fällen prägt sich das Kinking der V. poplitea so stark aus, daß in bestimmten Körperhaltungen mit einer venösen Abflußbehinderung gerechnet werden muß.
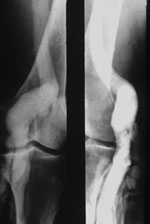 Ausgeprägte sekundäre Leitveneninsuffizienz bei einer 49-jährigen Frau mit Varikose seit dem 19. Lebensjahr. Rezidivierendes und zuletzt persistierendes Ulcus cruris seit 20 Jahren. Chronische venöse Insuffizienz im Stadium III. Schwere sekundäre Leitveneninsuffizienz mit Dilatation, Elongation und Verlust der Klappenfunktion in der popliteo-femoralen Strombahn. Darstellung durch aszendierende Pressphlebographie, links bei Innenrotation von 30°, rechts im seitlichen Strahlengang.
Ausgeprägte sekundäre Leitveneninsuffizienz bei einer 49-jährigen Frau mit Varikose seit dem 19. Lebensjahr. Rezidivierendes und zuletzt persistierendes Ulcus cruris seit 20 Jahren. Chronische venöse Insuffizienz im Stadium III. Schwere sekundäre Leitveneninsuffizienz mit Dilatation, Elongation und Verlust der Klappenfunktion in der popliteo-femoralen Strombahn. Darstellung durch aszendierende Pressphlebographie, links bei Innenrotation von 30°, rechts im seitlichen Strahlengang.
Bei der schweren SLVI ist die V. femoralis superficialis erweitert, und sie nimmt einen geschlängelten Verlauf an. Die Störung der Hämodynamik kommt bei der Phlebographie durch den Verwaschungseffekt zum Ausdruck (7). Infolge der Gefäßdilatation schließen die Venenklappen in der popliteo-femoralen Strombahn nicht mehr ab. Dadurch verliert die Wadenmuskelpumpe ihre Funktion und die Blutsäule vermischt sich in stärkerem Maße mit kontrastmittelfreiem Blut. Die Röntgenbilder nehmen den Aspekt wie bei einer schlechten Untersuchungstechnik an.
Die Leitvenen des Unterschenkels zeigen phlebographisch bei der SLVI einen suffizienten Klappenapparat. Eine diskrete Erweiterung ihrer Gefäßlumina wirkt sich hämodynamisch offenbar nicht aus. Das ist aus pathophysiologischen Überlegungen auch leicht erklärbar: Die V. poplitea und die V. femoralis superficialis haben nur zwei bis drei Venenklappen und reagieren deshalb auf jede hämodynamische Veränderung viel sensibler als die Unterschenkelgefäße, bei denen sich entsprechende Effekte auf mindestens fünf Leitvenen mit jeweils 5 oder mehr Venenklappen verteilen, insgesamt also auf etwa 25 Venenklappen. Ein Seil, das aus vielen dünnen Fasern besteht, ist wesentlich stabiler als das Seil aus einer einzelnen dicken Faser. Außerdem werden die kruralen Leitvenen durch die engen Kompartments besser geschützt.
In der V. femoralis superficialis nimmt der retrograde Flow bei der SLVI unter dem Valsalva-Test nach distal hin kontinuierlich ab, bis es an den tiefen Venen des Unterschenkels zu überhaupt keiner rückwärtigen Blutbewegung mehr kommt. Auch das läßt bei der Preßphlebographie gut erkennen, allerdings bei der retrograden Preßphlebographie mit Injektion des Kontrastmittels in die Leistenvene. Damit liegt ein grundlegender Unterschied zum postthrombotischen Syndrom mit vollständigen Rekanalisation und Zerstörung der Venenklappen vor. Beim schweren postthrombotischen Syndrom und bei der kongenitalen Aplasie sind nämlich auch die Leitvenen des Unterschenkels betroffen und erlauben ein unbegrenztes Pooling des venösen Blutes zur Peripherie hin.
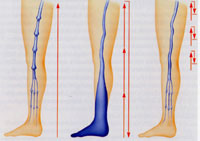 Schematische Darstellung der Strömungsbedingungen in den tiefen Leitvenen bei antegrader und retrograder venöser Insuffizienz.
Schematische Darstellung der Strömungsbedingungen in den tiefen Leitvenen bei antegrader und retrograder venöser Insuffizienz.Links: Normale Verhältnisse entsprechend dem dynamischen Zyklus von Arnoldi.
Mitte: Retrograde Strömungsinsuffizienz. In der Systole kräftiger antegrader Flow, oftmals aber auch verminderung durch gleichzeitige antegrade Insuffizienzanteile. In der Diastole unerschöpfliche retrograde Strömung in Orthostase und beim Valsava-Test.
Rechts: Antegrade Strömungsinsuffizienz. Eingeschränkte Drainage und Pumpfunktion durch Ausfall oder Überforderung der peripheren Venenpumpen.
| Tabelle 2: Formen der Leitveneninsuffizienz |
| Antegrad | Sekundäre Leitveneninsuffizienz |
| Arteriovenöse Fistel | |
| Funktionsausfall der peripheren Muskelpumpen | |
| Retrograd | Postthrombotisches Syndrom |
| Kongenitale Venenklappenaplasie |
Bei der SLVI haben wir es mit der antegraden Strömungsinsuffizienz zu tun. Schneider und Fischer nahmen bei der schweren Varikose eine Insuffizienz der Wadenmuskelpumpe an (19). Darin liegt wohl letztendlich auch der Schlüssel zur Pathogenese des Krankheitsbildes der SLVI. Die Muskelpumpe reicht nicht aus, um das retrograd über die variköse Stammvene anflutende Blutvolumen in der vorgegebenen Situation zu bewältigen. Das Blut kann durch die Muskelarbeit nicht aus dem Bein herausgeschafft werden. Dafür spricht auch, daß die Krankheit bei einer Stammvarikose der V. saphena parva in der gleichen Weise anzutreffen ist, wenn auch infolge der geringeren Blutvolumina in einer leichteren Ausprägung.
Bei der kräftigen körperlichen Bewegung funktioniert die Dynamik des Blutstroms auch bei der SLVI noch wesentlich besser als im Stehen mit entspanntem Bein. Hierbei treten dann auch die Beschwerden des Patienten in besonderem Maße auf.
Wann und in welchem Ausmaß sich die SLVI im Verlauf der Krampfaderkrankheit entwickelt, ist großen individuellen Schwankungen unterworfen (Tab. 3).
| Tabelle 3: Faktoren zur Begünstigung der sekundären Leitveneninsuffizienz |
| Topographie des distalen Insuffizienzpunktes am Unterschenkel oder Fuß |
| Sportliche Inaktivität |
| Orthostatische Belastung |
| Immobilität der großen Gelenke |
| Hormonelle Einflüsse |
| Genetische Faktoren |
Die größte Bedeutung kommt der Lokalisation des distalen Insuffizienzpunktes zu. Je tiefer er liegt, je stärker also die Stammvarikose (entsprechend dem Stadium III oder IV) ausgeprägt ist, um so größer muß das retrograd transportierte Blutvolumen sein. Unterhalb vom distalen Insuffizienzpunkt zieht dann die konjugierende Seitenastvarikose in die Peripherie. Infolge ihrer starken Schlängelung bremst sie den Rückfluß ab. Je länger diese Seitenastvarikose ist, um so stärker erfolgt auch die Verminderung des retrograden Blutflusses in der Zeiteinheit. Der Rezirkulationskreis I, der dem klinischen Bild einer Seitenastvarikose der V. saphena accessoria lateralis entspricht, führt praktisch nie zur SLVI und damit auch nicht zum chronischen venösen Stauungssyndrom.
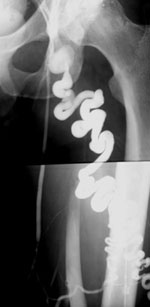 Stammvarikose der V. saphena magna im Stadium 1, entsprechend einer Seitenastvarikose der V. saphena accessoria lateralis. Durch die starke Schlängelung der Krampfader werden die Geschwindigkeit und damit das Volumen des retrograden Rückflusses stark vermindert. Eine Überlastung der tiefen Venen entsteht deshalb nicht. Es kommt praktisch nie zur chronischen venösen Insuffizienz, wie stark die Varikose auch ausgeprägt sein mag.
Stammvarikose der V. saphena magna im Stadium 1, entsprechend einer Seitenastvarikose der V. saphena accessoria lateralis. Durch die starke Schlängelung der Krampfader werden die Geschwindigkeit und damit das Volumen des retrograden Rückflusses stark vermindert. Eine Überlastung der tiefen Venen entsteht deshalb nicht. Es kommt praktisch nie zur chronischen venösen Insuffizienz, wie stark die Varikose auch ausgeprägt sein mag.
In gegenteiliger Weise bewirkt der Rezirkulationskreis IV mit einer Stammvarikose der V. saphena magna von der Leiste bis zum Fuß sofort eine schwere periphere Stauungssymptomatik, und das Ulcus cruris tritt schon im jugendlichen Alter auf.
Entsprechende Erfahrungen sind aus der Landschaftsökologie bekannt.
 Austrocknung der Everglades/USA durch die Anlegung von geraden zementierten Kanälen. Die gerade Linienführung erlaubt eine hohe Flussgeschwindigkeit und bewirkt viel höhere Strömungsvolumina in den Kanälen als in den ursprünglichen, stark gewundenen Bächen, die das Wasser halten und die ursprüngliche Landschaft bewahren (Aus Der Spiegel 1989)
Austrocknung der Everglades/USA durch die Anlegung von geraden zementierten Kanälen. Die gerade Linienführung erlaubt eine hohe Flussgeschwindigkeit und bewirkt viel höhere Strömungsvolumina in den Kanälen als in den ursprünglichen, stark gewundenen Bächen, die das Wasser halten und die ursprüngliche Landschaft bewahren (Aus Der Spiegel 1989)Der stark geschlängelte Bach („Seitenast“) vermag nur eine relativ begrenzte Menge des anfallenden Regens abzutransportieren, Wiesen und Sümpfe behalten ihre Feuchtigkeit und bewahren den Fluß („tiefe Leitvene“), in den der Bach einmündet, vor der Überschwemmung. Der gradlinig durchgezogene Kanal („V. saphena magna“) führt dagegen hohe Wasserkapazitäten ab, trocknet die Landschaft aus und zerstört die Natur wie in den Pontinischen Sümpfen oder den Everglades. Die abführenden Flüsse und Ströme, zu denen der Kanal hinführt, werden überflutet („Leitveneninsuffizienz“).
Einen wichtigen protektiven Faktor der SLVI stellt offenbar die sportliche Betätigung dar. Kräftige und häufige Aktivierungen der peripheren Venenpumpen können hohe Blutvolumina bewältigen. Beim flotten Wandern, Joggen, Fahrradfahren oder Schwimmen nimmt die periphere Schwellungsneigung ab. Der Leistungssportler kann durchaus große Krampfadern entwickeln, er bekommt aber seltener die SLVI. Seine tiefen Leitvenen sind an hohe Transportkapazitäten angepasst. Andererseits bleiben in der Orthostase, also beim Stehen mit mehr oder weniger entspannter Wadenmuskulatur die angesammelten Blutvolumina im Bein liegen und werden von der Muskelpumpe nicht abgeschöpft. Auch die Bewegungseinschränkung in den großen Gelenken der Extremität wirkt der physiologischen Hämodynamik entgegen.
Weiterhin können sich hormonelle Einflüsse in nachteiliger Weise auswirken. Östrogene haben einen allgemein gefäßdilatierenden Effekt. Ohne Zweifel muß auch der genetischen Determination eine wichtige Rolle zuerkannt werden. Vielleicht gehört in diesen Bereich auch eine sogenannte primäre Leitveneninsuffizienz hinein, ein nicht näher definiertes Krankheitsbild mit unsicherer Beziehung zu regressiven Veränderungen am Venensystem.
Abgesehen vom distalen Insuffizienzpunkt ist die Bedeutung der einzelnen Risikofaktoren für den Krankheitsverlauf der SLVI bisher statistisch nicht belegt und individuell nicht abzuschätzen. Deshalb bleiben auch prognostische Aussagen, ob und wann es im Einzelfall zur Dekompensation des Rezirkulationskreises kommt, unsicher.
In der speziellen klinischen Diagnostik kommt es zunächst darauf an, die SLVI objektiv zu dokumentieren. Auf dem Ausschluß oder dem Nachweis basiert heute die grundlegende Einteilung der Krampfaderkrankheit in die unkomplizierten und in die komplizierten Formen (Tab. 4).
| Tabelle 4: Syndrome im Rahmen der Krampfaderkrankheit |
| Unkomplizierte Krampfaderkrankheit |
| Komplizierte Krampfaderkrankheit |
| Chronische venöse Insuffizienz |
| Arthrogenes Stauungssyndrom |
| Chronisches venöses Faszienkompressionssyndrom |
Daraus sind wichtige therapeutische Konsequenzen abzuleiten. Zum zweiten kommt es auf die Quantifizierung der pathomorphologischen und pathophysiologischen Veränderungen an.
Klinische Diagnostik
Die klinische Symptomatik der SLVI entspricht dem chronischen venösen Stauungssyndrom, mit anderen Worten, der chronischen venösen Insuffizienz (CVI). Wir haben anhand des Symptoms Gewebssklerose die Einteilung der CVI in 4 Stadien vorgeschlagen (Tab. 5).
| Tabelle 5: Einteilung der chronischen Insuffizienz aufgrund der Gewebssklerose |
| Stadium I | keine Sklerose |
| Stadium II | Dermatoliposklerose |
| Stadium III | Dermatolipofasciosclerosis regionalis |
| Stadium IV | Dermatolipofasciosclerosis circularis |
| (Chronisches venöses Faszienkompressionsyndrom) |
Wenn andere Krankheiten der peripheren Gefäße, Störungen der Statik oder Traumata wegfallen, darf jedes lokalisierte Ödem bei einem Rezirkulationskreis als Hinweis auf seine Dekompensation interpretiert werden (Stadium I der CVI). Man wird zu dieser Erkenntnis überraschend häufig gelangen.
Später im Krankheitsverlauf treten die Dermatoliposklerose (Stadium II) und dann die Dermatolipofasziosklerose (Stadium III und IV der CVI) hinzu. In jedem Stadium kann es zur Ausbildung eines Ulcus cruris kommen. Letztendlich wird also durch die sekundäre Leitveneninsuffizienz der Weg in die CVI, in das arthrogene Stauungssyndrom oder ausnahmsweise sogar in das chronisch venöse Faszienkompressionssyndrom geebnet (9).
Bildgebende Verfahren
Recht verläßliche Informationen über die Dynamik in den tiefen Leitvenen bei der SLVI sind durch die moderne Duplexsonographie zu erhalten (13). Unter dem Valsalva-Test strömt das Blut in der Leistenregion nicht nur in die V. saphena magna, sondern auch in die V. femoralis superficialis und in die V. profunda femoris sowie in die vielen kleine Nebenenäste zurück (Abbildung 9a). Im Bereich des Oberschenkels ist bei der Untersuchung am stehenden Patienten das antegrade Strömungssignal des Wadenkompressionstests pathognomonisch verändert (Abbildung 9b).
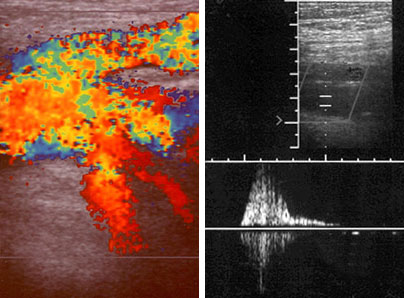 Duplexsonographie bei Stammvarikose der V. saphena magna und sekundärer Leitveneninsuffizienz. 59-jährige Frau mit jahrzehntelanger Anamnese.
Duplexsonographie bei Stammvarikose der V. saphena magna und sekundärer Leitveneninsuffizienz. 59-jährige Frau mit jahrzehntelanger Anamnese.a. Leistenregion. Beim Preßversuch retrograde Strömung nicht nur in den Saphenastamm, sondern auch in die V. femoralis superficialis, in die V. profunda femoris und in Seitenäste der Krosse.
b. Wadenkompressionstest über der V. femoralis superficialis. Antegrade Strömungsinsuffizienz. Breitbasiges, abgestumpftes Signal nach proximal und distal. Bei Dekompression kurzer Reflux.
Die SPFI ist auch heute noch in der Hauptsache eine phlebographische Diagnose. Die röntgenmorphologischen Veränderungen sind hauptsächlich in der popliteo-femoralen Region ausgeprägt. Dazu gehören die Erweiterung der Strombahn mit dem Verlust der Klappenfunktion, die Abwinkelung des popliteo-femoralen Übergangs und die vermehrte Schlängelung der V. femoralis superficialis. In den Leitvenen des Unterschenkels oder in der Beckenregion treten die Veränderungen weniger deutlich oder überhaupt nicht in Erscheinung. Eine Ausnahme bildet noch die sekundäre Tibialveneninsuffizienz, eine regionäre Komplikation bei der schweren Cockettschen Perforansinsuffizienz (7).
Auf die hämodynamische Bedeutung des Verwaschungseffekts der Kontrastmittelsäule wurde schon aus pathophysiologischer Sicht eingegangen. Mit dem Leitvenentest nach Hach läßt sich der Schweregrad einer SLVI semiquantitativ erfassen. Normalerweise fließt das Blut in der popliteo-femoralen Achse bei manueller Kompression der Wade schlagartig ab. Mit zunehmender SLVI müssen zwei, drei oder mehrere Kompressionsmanöver vorgenommen werden, um unter den Bedingungen der aszendierenden Preßphlebographie in der entspannten Schräglage des Patienten auf dem Röntgentisch die Leistenregion darzustellen (7).
Physikalische Messungen
Eine beweiskräftige Dokumentation der SLVI liefert die periphere Phlebodynamometrie. Perthes beobachtete schon 1895, dass der dynamische Venendruck bei Patienten mit schwerer Varikose weniger stark absinkt als bei gesunden Probanden. Die Verhältnisse ließen sich durch die Kompressionstherapie und durch therapeutische Ausschaltung der Krampfadern normalisieren (17). Als wichtige Parameter gelten der Druckabfall P und die Druckausgleichszeit P2. Lechner und Hach (18) haben 1978 an einem phlebographisch kontrollierten Kollektiv beobachteten können, dass sich pathologische Werte des Venendrucks nach der chirurgischen Therapie der schweren Stammvarikose infolge der SLVI nicht sofort ausgleichen. Heute darf die periphere Phlebodynamometrie für die Quantifizierung der Krankheit vor und nach Therapie herangezogen werden, wenn es im speziellen um funktionelle Zusammenhänge geht.
Die Einschränkung der Pumpfunktion der Muskulatur wird auch mit der Photoplethysmographie erfasst.
Die Varikose der extrafaszialen Venen und die Dilatation der intrafaszialen Gefäße bewirken eine Erhöhung der venösen Kapazität. Da bei der SLVI keine strukturellen Strömungshindernisse vorliegen, ist auch die Drainagefunktion erhöht. In extremen Fällen können die Werte das Doppelte der Norm ausmachen.
Durch die physikalischen Messungen besteht die Möglichkeit, den Verlauf der SLVI über den Zeitraum von Jahren zu kontrollieren.
Das Behandlungsprinzip bei der SLVI kann nur in der Ausschaltung des extrafaszialen Rezirkulationskreises bestehen. Als Therapie der Wahl gilt die komplette Sanierungsoperation mit partieller Saphenaresektion, Exhairese der konjugierenden Seitenastvarikose und selektiver Perforansdissektion. Stranzenbach und Hach haben 1991 eine Reihe von Patienten, die sich dem Eingriff unterzogen hatten, nachuntersucht. Die Phlebographie zeigte eine signifikante Reduktion der Gefäßlumina im Vergleich zur Ausgangssituation. Bei günstigen Voraussetzungen werden die Klappen auch wieder schlußfähig und es kommt zur Restitutio ad integrum (22). Über die Valvuloplastik im Rahmen der SLVI liegen keine systematischen Erfahrungen vor.
Eine dauerhafte Ausschaltung der Stammvarikose durch die Sklerosierung gelingt nur bei alten Menschen. Scheinbare Heilungen durch die Verödung haben aber eine große praktische Bedeutung. Die konjugierende Seitenastvarikose verschwindet zwar, sie wird aber durch andere Abflußwege unterhalb des distalen Insuffizienzpunktes ersetzt. Der Rezirkulationskreis bleibt bestehen. Die Krankheit schreitet fort und führt gelegentlich zum Ulcus cruris, ohne dass der Patient auf den ersten Blick größere Krampfadern erkennen lässt. Durch die Duplexsonographie wird sofort eine Klärung herbeigeführt.
Die Therapie mit Kompressionsstrümpfen vermag eine schwere Stammvarikose nicht zu beeinflussen. Gerade in dem wichtigsten Bereich des Oberschenkels, wo die Veränderungen der SLVI am stärksten ausgeprägt sind, wirkt sich der Andruck des Strumpfes nicht so stark aus, dass die V. saphena magna hämodynamisch ausgeschaltet wird.
Nach erfolgreicher Operation ist die physikalische Nachbehandlung der SLVI mit dem Training der peripheren Venenpumpen von großer Bedeutung. Dazu sind Krankengymnastik, Gefäßsport und jede andere entsprechende sportliche Aktivität geeignet. Bei einer persistierenden Schwellungsneigung wird auch das weitere Tragen des Kompressionsstrumpfes der Klasse II A-D empfohlen. Sobald aber schon die Störungen der Mikrozirkulation mit einem chronischen venösen Stauungssyndrom eingetreten sind, muss zusätzlich die paratibiale Fasziotomie nach der Hach´schen offenen Operationsmethode (5) oder dem endoskopischen Verfahren nach Hauer (12) in Erwägung gezogen werden.
Die theoretischen Grundlagen für die Entstehung der sekundären Leitveneninsuffizienz wurden von Trendelenburg vor mehr als 100 Jahren erkannt. Erst unserer Zeit blieb es vorbehalten, die Krankheit in ihrer ganzen Bedeutung zu verstehen. Dazu hat die aszendierende Pressphlebographie den entscheidenden Anteil geleistet. Heute muss bei jedem Patienten mit einer relevanten Krampfaderkrankheit an die Dekompensation des Rezirkulationskreises gedacht werden. Die Objektivierung der Diagnose hat in mehrerer Hinsicht eine erhebliche Bedeutung. Der Patient erwartet therapeutische Konsequenzen hinsichtlich seiner gegenwärtigen Situation als auch für die Zukunft. Der Arzt muss also prognostische Aspekte in seine Beratung einbeziehen. An den Wissenschaftler ergeht der Auftrag, alle neuen Behandlungsmethoden wie Chiva oder die Valvuloplastik der V. saphena magna in ihrer Auswirkung auf die venöse Hämodynamik des tiefen Venensystems genauestens zu erforschen und durch adäquate Untersuchungsmethoden zu belegen.
Literaturverzeichnis
1. Bjordal RI (1972) Blood circulation in varicose veins of the lower extremities. In: Die venöse Insuffizienz. Schneider KW (Hrsg). Baden Baden, Brüssel: Witzstrock 110-3
2. Dyszynski TJ, Marshall M, Lewandowski Z (1999) Innendurchmesser der Vena femoralis communis als diagnostischer und prognostischer Parameter für die CVI. Phlebol 28:126-31
3. Fischer H, Siebrecht H (1970) Das Kaliber der tiefen Unterschenkelvenen bei der primären Varikose und beim postthrombotischen Syndrom (eine phlebographische Studie). Hautarzt 21: 205-9
4. Hach W (1981) Spezielle Diagnostik der primären Varikose. Gräfelfing: Demeter. S 65-153
5. Hach W (1987) Indikation und Kontraindikation der paratibialen Fasziotomie. In: Die klinische Bedeutung der Venae perforantes. Ergebn Angio Bd 34. Cockett F, Klüken N (Hrsg). Stuttgart, New York: Schattauer. S 61-9
6. Hach W (1988) Neue Aspekte zum Spontanverlauf einer Stammvarikose der V. saphena magna. Phleb u Proktol 17:79-82
7. Hach W, Hach-Wunderle V (1994) Phlebographie der Bein- und Beckenvenen. Berlin, Heidelberg, New York, Tokio: Springer. S 94-106
8. Hach W, Hach-Wunderle V (1994) Die Rezirkulationskreise der primären Varikose. Springer. Heidelberg. S 41-8
9. Hach W, Hach-Wunderle V (2000) Die Graduierung der chronischen venösen Insuffizienz. Gefäßchirurgie 5:255-61
10. Hach W, Schirmers U, Becker L(1980) Veränderungen der tiefen Leitvenen bei einer Stammvarikose der V. saphena magna. In: Mikrozirkulation und Blutrheologie. Müller-Wiefel H (Hrsg). Baden Baden, Köln, New York: Witzstrock. S 468-70
11. Hach-Wunderle V (1992) Die sekundäre Popliteal- und Femoralveneninsuffizienz. Phlebol 21:52-8
12. Hauer G (1988) Endoskopische Perforansdissektion. Langenbecks Arch Klin Chir Suppl II (Kongreßbericht). S 157-60
13. Krünes U, Habscheid W (2000) Stellenwert von Ultraschallverfahren in der phlebologischen Diagnostik. Phlebol 29:146-53
14. Lechner W, Hach W (1978) Vergleichende Untersuchungen mit der peripheren Phlebodynamometrie und der aszendierenden Pressphlebographie bei Erkrankungen des extrafaszialen Venensystems. In May R, Kriessmann A: Periphere Venendruckmessung. Thieme. Stuttgart. S 69-70
15. Mellmann J (1981) Morphometrie der Beinvenen und periphere Phlebodynamometrie bei primärer Varikose. Phlebol u Proktol 10: 65-120
16. Neugebauer J (1989) Zur Existenz der Leit- und Muskelveneninsuffizienz bei primärer Varikose. Phebol u Proktol 18: 62-3
17. Perthes G (1895) Ãœber die Operation der Unterschenkelvarizen nach Trendelenburg. Dtsch Med Wschr 21: 253-7
18. Recek C (2001) Venöse Hämodynamik in den Beinen bei Gesunden und bei primärer Varikose. Phlebol 30:107-14
19. Schneider W, Fischer H (1969) Die chronisch-venöse Insuffizienz. Stuttgart. Enke. S 59
20. Schoop W (1974) Pathophysiologie der Arterien und der arteriellen Durchblutung. In: Angiologie. Heberer F, Rau G, Schoop W (Hrsg). Stuttgart: Thieme.33-87
21. Stranzenbach W, Hach W (1990) Diagnostik der sekundären Popliteal- und Femoralveneninsuffizienz bei Stammvarikose. Vasa 19: 30-4
22. Stranzenbach W, Hach W (1991) Phlebographische Verlaufsbeobachtungen der sekundären Popliteal- und Femoralveneninsuffizienz bei Stammvarikose. Phlebol 20: 25-9
23. Trendelenburg F (1891) Ãœber die Unterbindung der V. saphena magna bei Unterschenkelvarizen. Bruns' Beitr Klin Chir 7: 195-210
zum Anfang
zurück

